规范化、规模化、集中化是药包材行业发展趋势
1、行业发展概况
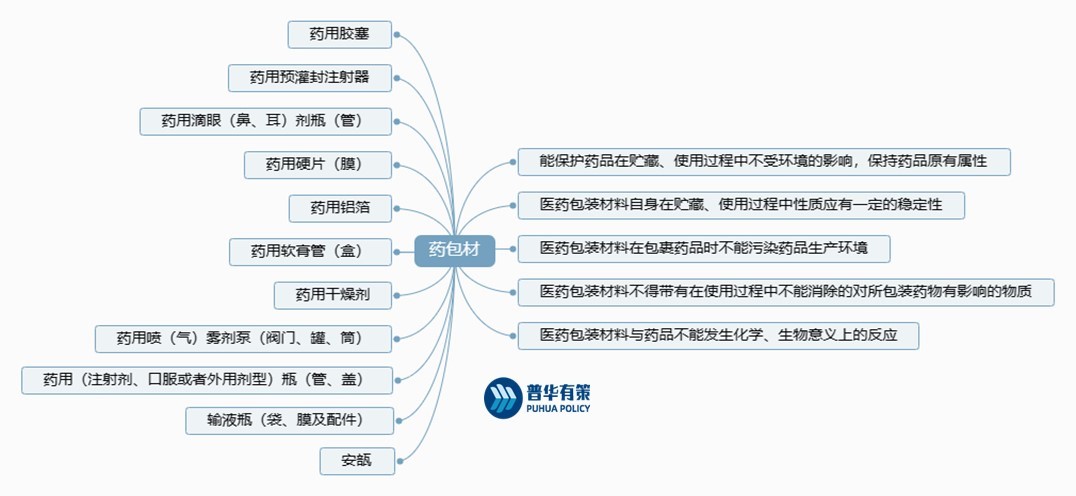
在药品的包装、贮藏、运输和使用过程中,药品包装的材料与结构形式,尤其是直接接触药品的包装材料,对保证药品安全性、稳定性起决定性作用。根据国家食药监局2004年制定公布的《实施注册管理的药包材产品目录》,药包材的注册品种类别共11类。
我国药包材的监管经历了企业生产许可、产品注册审批与药品制剂关联审评审批三个阶段。经过十多年的药包材产品单独注册制度之后,2015年至今,《关于改革药品医疗器械审评审批制度的意见》、《关于药包材药用辅料与药品关联审评审批有关事项的公告》、《关于进一步完善药品关联审评审批和监管工作有关事宜的公告》等规范性文件先后出台,将原有的药包材独立审批制度修改为关联审评审批制度。药品制剂注册申请与已登记原辅包进行关联,药品制剂获得批准时,即表明其关联的原辅包通过了技术审评,登记平台标识为“A”;未通过技术审评或尚未与制剂注册进行关联的标识为“I”。
经过多年的发展,我国医药包装材料行业得到了较大的进步,市场规模已达到1000亿元。行业在竞争格局上呈现出企业数量众多、大型企业与中小型企业并存、经营分散、竞争充分等特点。目前我国各类药包材生产企业1500余家,国内包括山东省药用玻璃股份有限公司、肖特中国、重庆正川医药包装材料股份有限公司、西安环球印务股份有限公司、上海海顺新型药用包装材料股份有限公司等大型生产企业占据了行业的较大市场份额,头部企业的龙头效应较为明显。随着国家供给侧改革深入开展、监管体制的进一步完善和监管要求的提升,技术水平较低、规范意识较差的企业将逐步被市场环境所淘汰,行业的规范程度、技术水平将得到进一步的提升,规范化、规模化、集中化是行业的发展趋势。
2、行业发展趋势
(1)国家政策、高端药品对医药包装材料的提出了更高的要求
在药品质量监管日趋严格以及公众对药品安全日益重视的背景下,制药企业对医药包装材料的质量要求不断提升,由追求低成本向追求高质量、高稳定性转变,在选择医药包装材料时将更加关注质量是否稳定、与药品的相容性等各项指标是否达标。《产业结构调整指导目录(2019年本)》已将化学稳定性好、可降解,具有避光、高阻隔性的功能性材料,药品包装材料纳入重点推进发展和鼓励类发展领域。
此外,国内外处于临床前、中、后研究开发的各类生物制药、疫苗(包括新冠疫苗)、抗癌、抗菌、抗肿瘤、单抗、蛋白类等高端注射剂药品的研发过程和制造工艺较为复杂,不同剂型、品种、规格的药品对医药包装材料的高阻隔性、相容性、稳定性等均提出了更复杂的需求。
(2)行业集中趋势进一步加强
目前,药品和药包材实施关联审评审批制度,药品上市许可持有人成为药品质量管理体系的责任主体,承担药品全生命周期的质量管理责任。
为保证制药企业所研发生产的药品、制剂成功通过监管部门审核、注册并且在后续生产中不出现质量问题,药企会强化供应商现场审核,在选择医药包装材料供应商时会倾向于综合实力较强、技术水平领先、规模化生产能力强、产品质量稳定、品牌知名度高的行业领先企业。未来规模较小、技术较为落后、生产工艺不规范、产品质量较差的医药包装材料企业将会逐步被市场淘汰,而行业内龙头企业通过企业并购、新项目建设等方式来进一步扩大自身规模,抢占更多的市场份额,行业集中度将进一步提高。
3、行业壁垒

更多行业资料请参考普华有策咨询《2023-2029年药包材行业市场调研及发展趋势预测报告》,同时普华有策咨询还提供产业研究报告、产业链咨询、项目可行性报告、项目后评价报告、十四五规划、BP商业计划书、产业图谱、产业规划、蓝白皮书、IPO募投可研、IPO工作底稿咨询等服务。(PHPOLICY:LDL)